Lietuvos mokslų akademijos pozicija dėl COVID-19 Lietuvoje
Prof. Vytautas Usonis, akad. prof. Vaidutis Kučinskas, doc. dr. Tomas Kačergius, dr. Silvija Kiverytė, akad. prof. Aurelija Žvirblienė, prof. Vytautas Kasiulevičius, prof. Ligita Jančorienė

Santrauka
Apie SARS-CoV-2 genomą yra sukaupta daug informacijos. Vienas įdomiausių šio genomo požymių yra S (smaigo) baltymo genai ir su juo susiję mutacijos. S genas lemia viruso baltymo struktūrą, kuri nusako jo prisijungimą prie žmogaus ląstelės paviršiuje esančio ACE2 receptoriaus. SARS-CoV-2, kaip RNR turintis virusas, pasižymi santykinai dideliu mutacijų dažniu; 2020 m. įvairiose pasaulio šalyse identifikuotos naujos viruso atmainos, plintančios visame pasaulyje. Šios mutacijos, įvykusios S (smaigo) baltymą koduojančiame gene, padidino SARS-CoV-2 viruso infektyvumą ir nulėmė jo spartesnį plitimą žmonių populiacijoje.
Šiuo metu yra du pagrindiniai tyrimai, nustatantys, ar asmuo yra užsikrėtęs SARS-CoV-2: viruso nukleorūgščių (RNR) aptikimas (PGR) ir viruso antigeno nustatymas. PGR tyrimui naudojami šie ėminiai: tepinėliai iš nosiaryklės, ryklės ir nosies landų. Jie tiriami individualiai arba kaupiniuose. PGR metodu viruso RNR gali būti aptinkamos kvėpavimo takuose likus 2 dienoms iki simptomų atsiradimo, jos aptinkamos ir per 7–10 dienų nuo simptomų pradžios. Antigenų testai nėra tokie jautrūs kaip PGR testai. Antigenų aptikimo
laikotarpis yra trumpesnis negu RNR. Masiniam testavimui greitųjų antigeno testų reikėtų vengti.
Pasaulis jau turi ginklą prieš SARS-CoV-2 – vakcinas, keturios iš jų užregistruotos Europos vaistų agentūroje (EVA). Šių vakcinų III fazės klinikiniai tyrimai, kuriuose dalyvavo dešimtys tūkstančių tiriamųjų, įrodė jų saugumą ir aukštą veiksmingumą apsaugant nuo simptominės COVID-19 ligos. Jos sukurtos naudojant skirtingas technologines platformas: vakcinos, kurių sudėtyje yra informacinė RNR, arba vakcinos, kurių sudėtyje yra nesidauginantys adenovirusai su įterptu SARS-CoV-2 S baltymo genu. Kuriamos ir kitų platformų vakcinos, tačiau jos dar nėra registruotos. Pradėjus gyventojų skiepijimą, gaunama vis daugiau duomenų apie vakcinų veiksmingumą realiomis sąlygomis apsaugant nuo simptominės COVID-19 ligos, sunkių komplikacijų ir mirties. Realiomis sąlygomis stebimas vakcinų veiksmingumas reikšmingai papildo klinikinių tyrimų duomenis.
Lietuvos įdirbis skiepijant prieš COVID-19 yra reikšmingas: sukurta vakcinų prieš COVID-19 tiekimo sistema, visoje šalyje įkurti skiepijimo punktai, paskiepyta didžioji dalis medikų bei didžiausios rizikos grupėms priskiriamų asmenų, bent viena doze paskiepyta daugiau nei 560 tūkstančių Lietuvos žmonių, atlikta daug kitų darbų. Plėtojant visuotinį skiepijimą, būtina gerinti informacinį darbą. Pradedant skiepijimą buvo labai svarbi rizikos grupių skiepijimo strategija. Šio programos etapo tikslas – prioritetinių grupių apsauga, tačiau programą plėtojant, laikas pereiti prie lankstesnės strategijos, kuria būtų siekiama sukurti visuomenės imunitetą.
COVID-19 poveikis sveikatos apsaugos sistemai susijęs su smarkiai išaugusiu ambulatorinių kontaktų skaičiumi bei padidėjusiomis hospitalizacijos apimtimis. Pandemijos piko metu ne mažiau kaip 40 % visų sveikatos sistemos resursų panaudojama Covid-19 pacientų sveikatos priežiūrai, tačiau medicinos darbuotojai taip pat suserga – vidutiniškai Lietuvoje COVID-19 infekcija persirgo 26,5 % ligoninių darbuotojų.
Dėl sumažėjusio ambulatorinės ir stacionarinės grandies pajėgumo teikti paslaugas, taip pat dėl pacientų vengimo kreiptis į gydymo įstaigas mažiau atliekama prevencinių tikrinimų ir ankstyvos diagnostikos intervencijų. Optimizuota pagalba visose paslaugų teikimo grandyse sergantiesiems lėtinėmis neinfekcinėmis ligomis turi užtikrinti stabilios pacientų būklės palaikymą, medikamentinio gydymo ir ambulatorinės priežiūros tęstinumą be lėtinių ligų paūmėjimų.
SARS-CoV-2 infekcija gali būti besimptomė ar pasireikšti lengva, vidutine, sunkia ir kritiškai sunkia COVID-19 ligos forma. Lietuvos gydymo įstaigose sukaupta didelė sergančiųjų COVID-19 gydymo patirtis. Sukurta racionalaus stacionarinių gydymo įstaigų resursų išdėstymo sistema. Apibrėžti pagrindiniai COVID-19 ligos etapai ir gydymo principai. Taikomi šiuolaikiniai ligos gydymo algoritmai, naudojamos pažangiausios gydymo priemonės.
SARS-CoV-2 genomo sandara
Genomas – tai organizmo baltymus koduojanti ir nekoduojanti genetinė informacija, įrašyta
ląstelės DNR (RNR) nukleotidų sekoje (Kučinskas, 2012). Lyginant įvairių organizmų genomus
yra akivaizdu, kad prokariotų (virusai, bakterijos) genomai yra sudaryti beveik tik iš koduojančių baltymus nukleotidų sekų, o eukariotų, ypač žmogaus, genomo baltymus koduojančios sekos sudaro tik apie 1,5 % viso genomo.
SARS-CoV-2 genomą sudaro viengrandė (ss)(+) ribonukleorūgštis (RNR: ACUG nukleotidai).
Jos detalų aprašą galima rasti NCBI genomo duomenų bazėje (NC 045512.2). Molekulė yra
sudaryta iš 29 903 nukleotidų, t. y. maždaug 30 tūkst. nukleotidų (29,9 kb).
Paveiksle pristatome tiesinę molekulės sandarą, bet iš tikrųjų ji yra žiedinė. Viršutinėje
dalyje pateiktas nukleotidų skaičius molekulėje nuo 0 iki 29 903, žemiau – kur ir kokie yra
genai. Tai įvairių ORF (atviro rėmelio skaitymo), S – smaigo, M – membranos, E – apvalkalo,
N – nukleokapsidės baltymų genai; TRS – informacijos nurašymą kontroliuojančios sekos, L –
lyderinė seka (pagal Kim et al., Cell, 2020, 181, 914–921), 5’ ir 3’ netransliuojamos sekos, o
pabaigoje – poli A uodega.

Galbūt vienas įdomiausių šio genomo požymių yra S (smaigo) baltymo genai ir su juo susiję
mutacijos. Būtent S genas lemia viruso baltymo struktūrą, kuri nusako jo prisijungimą prie
žmogaus ląstelės paviršiuje esančio ACE2 receptoriaus. Vienos mutacijos gali prisitvirtinimą
ir RNR patekimą į ląstelę padidinti, kitos – sumažinti. Apskritai SARS-CoV-2 genomas yra ypač
artimas BAT-CoV (šikšnosparnio) genomui, todėl manoma, kad virusas žmogui galėjo būti
perduotas iš šikšnosparnių. Kita vertus, tam yra reikalingas tarpininkas. Juo galėjo būti šuo,
nes šie gyvūnai gali apsikrėsti SARS-CoV-2. Dar daugiau – šuns ir žmogaus angiotenziną konvertuojančio fermento geno (ACE2) panašumas yra pribloškiantis.
SARS-CoV-2 evoliucija: naujieji SARS-CoV-2 variantai
SARS-CoV-2, kaip RNR turintis virusas, pasižymi santykinai dideliu mutacijų dažniu dėl nuo
RNR priklausomos RNR polimerazės (replikazės), dalyvaujančios jo replikacijoje, padarytų klaidų. Tačiau kitų RNR turinčių virusų atžvilgiu SARS-CoV-2 mutacijų dažnis yra mažesnis, pvz., jis
beveik perpus yra mažesnis, palyginti su gripo virusu. Daugiausia tą lemia tai, kad SARS-CoV-2
fermentas egzonukleazė (ExoN) atlieka korektūros funkciją, t. y. geba iš dalies atitaisyti viruso
replikacijos metu atsiradusias mutacijas jo genome. Nepaisant to, susidarę nauji viruso variantai dar yra veikiami šeimininko (žmogaus) organizmo imuninės sistemos. Taigi vyksta natūrali
atranka ir išlieka bei įsitvirtina tik tie viruso variantai, kurie dėl mutacijų nulemtų pokyčių
struktūriniuose baltymuose sugeba išvengti imuninio atsako. Būtent šie mechanizmai sąlygoja SARS-CoV-2 evoliuciją, vykstančią nuo pat COVID-19 pandemijos pradžios.
2020 m. sausio mėn. pabaigoje Kinijoje buvo identifikuota mutacija smaigo S baltymą
koduojančiame SARS-CoV-2 gene, nulėmusi dviejų pagrindinių D ir G šio viruso linijų susidarymą. Dėl šios mutacijos S (smaigo) baltymo polipeptidinės grandinės 614 pozicijoje amino
rūgštis aspartatas virto glicinu (D614G pokytis). Pabrėžtina, kad dėl šios mutacijos G linijos
virusai ~20 % greičiau plito žmonių populiacijoje, palyginti su D linijos virusais. Būtent G linijos virusai įsivyravo ir tapo dominuojantys Europoje ir JAV.
2020 m. rugsėjo mėn. Jungtinėje Karalystėje nustatytas naujas SARS-CoV-2 viruso variantas – B.1.1.7. Naujojo varianto ypatumas yra tas, kad jis turi daugines S geno mutacijas, nulėmusias tam tikrus funkcinius S baltymo pokyčius, t. y. 69–70 deleciją, 144 deleciją, N501Y, A570D, D614G, P681H, T716I, S982A ir D1118H. Vienas iš svarbiausių pokyčių yra asparagino
pasikeitimas į tiroziną S baltymo polipeptidinės grandinės 501 pozicijoje (N501Y). Šis pokytis yra lokalizuotas S (smaigo) baltymo prie receptoriaus prisijungiančiame domene. B.1.1.7 variantas pasižymi daug stipresniu gebėjimu prisijungti prie žmogaus ACE2 receptorių ir efektyviau užkrėsti ląsteles, palyginti su D ir G linijų variantais. Apskaičiuota, kad N501Y pokytis padidino SARS-CoV-2 infektyvumą 52 %, o bazinį reprodukcinį skaičių – 43–90 %, leisdamas virusui sparčiau plisti žmonių populiacijoje. Dabartiniu metu B.1.1.7 yra dominuojantis viruso variantas Jungtinėje Karalystėje ir sudaro apytiksliai 95 % visų naujų COVID-19 infekcijos atvejų šalyje. Be to, jis jau yra užregistruotas 125 pasaulio šalyse, įskaitant Lietuvą.
2020 m. gruodžio mėn. Pietų Afrikos Respublikoje identifikuota nauja SARS-CoV-2 viruso atmaina – B.1.351 variantas. Šis variantas taip pat turi daugines mutacijas S gene, nulėmusias pokyčius smaigo S (smaigo) polipeptidinėje grandinėje: L18F, D80A, D215G, 242–244 deleciją, R246I, K417N, E484K, N501Y, D614G ir A701V. B.1.351 variantas turi esminius pokyčius S (smaigo) baltymo prie receptoriaus prisijungiančiame domene: K417N, E484K ir N501Y, todėl jo infektyvumas yra padidėjęs 52 %, o plitimas žmonių populiacijoje – 2,5 karto didesnis, palyginti su pradiniais SARS-CoV-2 variantais. Dabartiniu metu B.1.351 variantas dominuoja
Pietų Afrikos Respublikoje ir yra užregistruotas 75 pasaulio šalyse, tarp jų ir Lietuvoje.
2020 m. gruodžio mėn. Brazilijoje nustatytas dar vienas naujas SARS-CoV-2 viruso variantas – P.1, pasižymintis dauginėmis mutacijomis S gene, nulėmusiomis pokyčius S (smaigo) baltymo polipeptidinėje grandinėje: L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G, H655Y, T1027I ir V1176F. Reikėtų atkreipti dėmesį į tai, kad šiame variante pagrindiniai pokyčiai taip pat yra lokalizuoti S (smaigo) baltymo prie receptoriaus prisijungiančiame domene: K417T, E484K ir N501Y. Dėl šios priežasties P.1 varianto infektyvumas yra padidėjęs 52 %, o plitimas žmonių populiacijoje – 1,4–2,2 karto didesnis, palyginti su pradiniais SARSCoV-2 variantais. Šiuo metu P.1 variantas dominuoja Brazilijoje, yra užregistruotas 41 pasaulio šalyje, tačiau Lietuvoje jis kol kas nėra nustatytas.
Be jau minėtų atsiradusių SARS-CoV-2 variantų, 2020 m. gegužės mėn. JAV Kalifornijos
valstijoje identifikuotas naujas variantas – CAL.20C, apimantis B.1.427 ir B.1.429 linijas.
Pastarasis viruso variantas taip pat turi mutacijas S gene, sąlygojusias pokyčius S (smaigo)
baltymo polipeptidinėje grandinėje: S13I, W152C, L452R ir D614G. Iš šių pokyčių svarbiausias
yra leucino pasikeitimas į argininą S baltymo polipeptidinės grandinės 452 pozicijoje (L452R),
kadangi jis yra lokalizuotas prie receptoriaus prisijungiančiame domene. Nustatyta, kad
L452R pokytis 18,6–24 % padidino viruso plitimą žmonių populiacijoje, palyginti su pradiniais
SARS-CoV-2 variantais. Iki šiol CAL.20C variantas yra nustatytas 29 pasaulio šalyse, Lietuvoje
jis dar nėra identifikuotas.
Apibendrinant galima teigti, kad visos šios aprašytos mutacijos, įvykusios S (smaigo) baltymą koduojančiame gene, ir jų nulemti pokyčiai S baltymo prie receptoriaus prisijungiančiame domene padidino SARS-CoV-2 viruso infektyvumą ir nulėmė jo spartesnį plitimą žmonių
populiacijoje.
SARS-COV-2 identifikavimo laboratoriniai tyrimai
Šiuo metu yra du pagrindiniai tyrimai, nustatantys, ar asmuo yra užkrėstas SARS-CoV-2:
1) viruso nukleorūgščių (RNR) aptikimas;
2) viruso antigeno nustatymas.
Viruso tyrimai (nukleorūgščių arba antigeno aptikimo testai) naudojami ūminei infekcijai diagnozuoti, o antikūnų tyrimai patvirtina (arba ne) ankstesnę (ir persirgtą) SARS-CoV-2
infekciją. Ląstelių kultūroje galima izoliuoti SARS-CoV-2 virusą, tačiau Jungtinių Amerikos
Valstijų Ligų kontrolės ir prevencijos centras (CDC) rekomenduoja klinikinėms laboratorijoms
to nebandyti, nebent tai būtų atliekama sertifikuotoje III biologinio saugumo (BSL-3) lygio
laboratorijoje.
Atliekant bet kuriuos laboratorinius tyrimus, jų rezultatų klinikinis tikslumas ar patikimumas priklauso nuo testo kokybinių charakteristikų, tokių kaip jautrumas ir specifiškumas,
taip pat nuo išankstinės tikimybės, kad asmuo serga COVID-19 liga, ir nuo COVID-19 infekcijos paplitimo populiacijoje. Šie parametrai kartu lemia, ar tyrimo rezultatas turėtų būti
aiškinamas kaip teisingas.
Šiuo metu rekomenduojamas ūminės ar esamos SARS-CoV-2 infekcijos diagnozavimo metodas yra nukleorūgščių amplifikacijos testas (arba PGR), kuris nustato ne mažiau kaip du
virusui specifinius RNR genų taikinius. Jei dėl viruso genų mutacijų vienas taikinys nebūtų
nustatomas, antrasis galėtų užtikrinti viruso nustatymą. Dažniausiai naudojami šie SARSCOV-2 viruso genai-taikiniai: nukleokapsidės (N) baltymą koduojantis genas, spyglio (smaigo – S, angl. – spike) paviršiaus glikoproteiną koduojantis genas, nuo RNR priklausančios RNR polimerazės (RdRp) baltymų genai ir atviro skaitymo rėmelio 1ab (ORF1ab) genas. Tikralaikės PGR metodu galima tirti simptomus turinčius pacientus, taip pat asmenis, kuriems nustatyta ar įtariama COVID-19 ekspozicija, ir asmenis iš vietovės, kurioje liga labai išplitusi. Amerikos Infekcinių ligų draugijos (IDSA) gairėse taip pat siūloma, kad pacientams, kurių PGR testas
neigiamas, tačiau yra didelis klinikinis įtarimas dėl COVID-19, turėtų būti atliekamas papildomas PGR tyrimas, kuris, manoma, padidins tyrimo jautrumą iki 17 %.
Lietuvoje šiuo metu PGR tyrimams naudojami šie ėminiai: tepinėliai iš nosiaryklės, ryklės, nosies landų, bronchoalveolinių nuoplovų ir seilių. Jie tiriami individualiai arba kaupiniuose.
Apatiniuose kvėpavimo takų mėginiuose (pvz. bronchoalveolinėse nuoplovose) tikimybė aptikti virusą didesnė, tačiau šie ėminiai retai naudojami tyrimams, nes juos paimti galima tik stacionare ir yra rizikingas medicininiam personalui dėl susidarančių aerozolių, pavyzdžiui, bronchoskopijos metu. Seilių mėginiai taip pat pripažįstami kaip tinkami ūminės COVID-19 ligos diagnostikai, jau atsirado validuotų PGR rinkinių, tačiau kol kas laikoma, kad trūksta platesnių mokslinių studijų, suteikiančių daugiau informacijos apie seilių ėminių PGR tyrimų atlikimą.
Svarbu žinoti, kad tikralaikės PGR metodu viruso nukleorūgštys gali būti aptinkamos kvėpavimo takuose 2 dienas iki simptomų atsiradimo, taip pat jos aptinkamos 7–10 dienų nuo simptomų pradžios, o po 10 dienų viruso nukleorūgščių aptikimo galimybė (tai koreliuoja ir su paciento užkrečiamumu) labai stipriai sumažėja.Tik labai nedidelė ligonių dalis (apie 5 %) išlieka PGR teigiami vieną mėnesį ar ilgiau. Dažniausiai tai būna imunosupresuoti, lėtinėmis ligomis sergantys asmenys. Būtina pabrėžti, kad viruso nukleorūgščių aptikimas nebūtinai reiškia, kad virusas yra gyvas ir kad pacientas yra užkrečiamas. Todėl PGR teigiamas atvejis turi būti vertinamas kompleksiškai atsižvelgiant į klinikinius simptomus, epidemiologinę anamnezę ir kitus laboratorinius bei instrumentinius tyrimus.
Klaidingai neigiamas PGR rezultatas gali būti dėl viruso mutacijų, dėl blogai paimto ir/arba blogai gabento ėminio, jeigu ėminys paimtas per anksti (pvz., inkubaciniame periode) arba per vėlai (pvz., ligos pabaigoje), taip pat galimos techninės priežastys, susijusios su laboratorijos darbu ar reagentais. Vienas ar keli neigiami rezultatai neatmeta COVID-19 infekcijos galimybės. Kai kurie autoriai siūlo papildomai atlikti išmatų PGR tyrimą SARS-COV-2 viruso nukleorūgštims nustatyti.
Yra mokslinių tyrimų, patvirtinančių, kad PGR teigiamas rezultatas gali pasikartoti vėliau ligos eigoje arba pasveikus, tačiau nėra įrodymų, kad tokie pacientai galėtų užkrėsti kitus asmenis.
Antigenų testai yra mažiau jautrūs nei PGR testai. Greitąjį antigenų testą sveikatos priežiūros įstaigose arba institucijose, kuriose susiduriama su didesne rizika užsikrėsti COVID-19 liga, besimptomiams asmenims periodiniam profilaktiniam testavimui rekomenduojama atlikti tik šiais atvejais: kai
1) tiriamas židinys,
2) nustatomas didelis paplitimas regione,
3) nėra
pakankamai PGR tyrimų pajėgumų. Masiniam testavimui greitųjų antigeno testų reikėtų vengti, ypač esant mažam ligos paplitimui. Tačiau siekiant padidinti testavimo apimtis, kai kuriose šalyse (iš dalies ir Lietuvoje) taikomi profilaktiniai antigenų tyrimai, kurie kartojami kas 3-4 dienas. Antigenų aptikimo laikotarpis yra trumpesnis už nukleorūgščių aptikimo laikotarpį, todėl antigenų testai COVID-19 ligos simptomų turintiems asmenims turėtų būti atliekami ne vėliau kaip per 5 paras nuo simptomų pradžios, o sąlytį su patvirtintu COVID-19 atveju turėjusiems asmenims – ne vėliau kaip per 7 paras po turėto sąlyčio.
Vakcinos nuo COVID-19
Praėjus daugiau nei metams nuo COVID-19 pandemijos pradžios, pasaulis jau turi ginklą prieš
SARS-CoV-2 – vakcinas. Iki 2021-04-14 Europos Komisija patvirtino 4 vakcinas nuo COVID-19,
kurios praėjo griežtą įvertinimo ir registracijos procedūrą Europos vaistų agentūroje (EVA), –
tai Comirnaty (Pfizer/BioNTech), Vaxzervia (AstraZeneca), Moderna ir Johnson&Johnson/
Janssen vakcinos. Šių vakcinų III fazės klinikiniai tyrimai, kuriuose dalyvavo keliasdešimt tūkstančių tiriamųjų, įrodė jų saugumą ir aukštą veiksmingumą sukeliant imuninį atsaką prieš
SARS-CoV-2 ir apsaugant nuo simptominės COVID-19 ligos.
EVA užregistruotų COVID-19 vakcinų taikinys yra SARS-CoV-2 paviršiaus glikoproteinas –
smaigo (S) baltymas. Šios vakcinos sukurtos naudojant skirtingas technologines platformas:
1 Vakcinos, kurių sudėtyje yra informacinė RNR (iRNR, angl. messenger RNA, mRNA), koduojanti SARS-CoV-2 S baltymą. Ši iRNR molekulė yra sintetinė, todėl kuriant vakciną
nenaudojamas nei virusas, nei žmogaus, nei gyvūnų ląstelės. Kad patektų į ląsteles ir
būtų geriau apsaugota nuo degradacijos, iRNR molekulė supakuojama į lipidinę kapsulę. Suleidus tokią vakciną, iRNR patenka į ląsteles, kuriose sintetinamas SARS-CoV-2 S
baltymas. Šis procesas vyksta ląstelės citoplazmoje dalyvaujant ribosomoms ir ląstelės fermentams. Susidaręs S baltymas sukelia imuninį atsaką, t. y. antikūnų susidarymą
ir T limfocitų aktyvaciją. Tokio tipo yra Comirnaty ir Moderna vakcinos.
2 Vakcinos, kurių sudėtyje yra nesireplikuojantys virusiniai vektoriai su įterptu SARSCoV-2 S baltymo genu. Tokio tipo vakcinų kūrimui naudojami modifikuoti nekenksmingi žmogaus arba beždžionių adenovirusai. Parenkami tokie adenovirusai, kurie nėra
plačiai paplitę populiacijoje, kad prieš juos nebūtų susidaręs imunitetas. Paskiepijus
tokia vakcina, žmogaus ląstelėse sintetinamas SARS-CoV-2 S baltymas, kuris sukelia
imuninį atsaką. Tokio tipo yra Vaxzervia ir Johnson&Johnson vakcinos bei Rusijoje pagaminta Sputnik V vakcina.
Adenovirusinių ir iRNR vakcinų sudėtyje nėra adjuvantų, t. y. medžiagų, sustiprinančių
vakcinų sukeliamą imuninį atsaką.
Pasaulyje kuriamos ir kitokios, tradicinio tipo, vakcinos:
1 Inaktyvuoto (negyvo) SARS-CoV-2 viruso pagrindu sukurtos vakcinos. Tokios vakcinos
užregistruotos ir jau naudojamos gyventojams skiepyti Kinijoje (Sinovac, Sinopharm),
Rusijoje (CoviVac). Inaktyvuotos vakcinos naudojamos su adjuvantais, kad sukeltų stipresnį imuninį atsaką. Skirtingų šaltinių duomenimis, šių vakcinų veiksmingumas svyruoja nuo 50 iki 90 %. Europoje taip pat kuriama tokio tipo vakcina (VLA2001, Valneva),
kuri jau išbandyta I ir II fazės klinikiniuose tyrimuose.
2 Baltyminės (subvienetinės) vakcinos, kurių sudėtyje yra rekombinantinis, genų inžinerijos būdu sukurtas SARS-CoV-2 S baltymas bei adjuvantai. Tokio tipo vakcinos kuriamos nuo 1990 m., jos plačiai naudojamos vaikų ir suaugusiųjų skiepijimui. Įmonės
Novavax sukurta COVID-19 vakcina jau išbandoma III fazės klinikiniuose tyrimuose.Užregistravus COVID-19 vakcinas ir pradėjus gyventojų skiepijimą, gaunama vis daugiau duomenų apie vakcinų veiksmingumą apsaugant nuo simptominės COVID-19 ligos, sunkių
komplikacijų ir mirties. Tokiose šalyse kaip Izraelis ir Jungtinė Karalystė, kur didelė visuomenės dalis jau paskiepyta bent viena vakcinos doze, SARS-CoV-2 infekcijos atvejų ir mirčių nuo COVID-19 skaičius sumažėjo keliasdešimt kartų. Škotijoje patvirtintas 85–94 % Comirnaty ir Vaxzervia vakcinų veiksmingumas išvengiant hospitalizacijos. Nors vis dar trūksta duomenų apie imuniteto trukmę po skiepijimo, buvo paskelbta, kad apsauga po dviejų Comirnaty vakcinos dozių trunka ne mažiau kaip 6 mėnesius. Atsiranda vis daugiau mokslinių duomenų, kad COVID-19 persirgusiems ir paskiepytiems asmenims jau po vienos vakcinos dozės nustatomas aukštas virusui specifinių antikūnų lygis. Taigi realiomis sąlygomis stebimas vakcinų veiksmingumas reikšmingai papildo klinikinių tyrimų duomenis.
Ar turime skiepijimo prieš COVID-19 programą?
Visai Europos Sąjungai įsimintina data – 2020 m. gruodžio 27 diena, kai buvo pradėtas plataus masto skiepijimas prieš COVID-19. Tai buvo naujas COVID-19 kontrolės žingsnis, kadangi
vakcinų skiepijimas atvėrė naują epideminio proceso valdymo kryptį: šalia jau esamo poveikio infekcijos plitimo kelių grandžiai atsivėrė galimybės veikti ir imliosios visuomenės kryptimi. Per praėjusį laiką padaryta labai daug: sukurta vakcinų prieš COVID-19 tiekimo sistema, visoje šalyje įkurti skiepijimo punktai, paskiepyta didžioji dalis medikų bei didžiausios rizikos grupėms priskiriamų asmenų, bent viena doze paskiepyta daugiau nei 560 tūkstančių Lietuvos žmonų, atlikta daug kitų darbų. Tai neabejotini pasiekimai, tačiau suprantame, kad tai tik kelio pradžia, yra neatliktų darbų, skiepijimo programą būtina plėtoti.
Prie nepakankamai atliktų darbų pirmiausia minėtinas netinkamas komunikavimas skiepijimo tema. Vertinant iš plataus masto skiepijimo programos perspektyvos, informacinis darbas traktuojamas kaip pirmasis programos etapas, pradedamas dar iki pirmųjų skiepijimų.
Vertinant COVID-19 situaciją pasaulyje ir Lietuvoje, šis darbas turėjo prasidėti dar 2020 m. rudenį. Jau tada atliekamose apklausose buvo nurodoma, kad apie trečdalis apklaustųjų pasigenda išsamesnės informacijos. Šiandien situacija kiek gerėja, tačiau dar nepakankamai, ypač turint omenyje atskiras mūsų visuomenės grupes, pavyzdžiui, kitakalbius ar vyresnio amžiaus žmones.
Rizikos grupių skiepijimas dažniausiai būna pirmasis plačios apimties skiepijimo programos etapas. Suprantama, visuomet svarbūs pirmieji žingsniai ir jiems parenkamos prioritetinės grupės. Teorija sako, kad tai turi būti valstybės funkcionavimui svarbios struktūros
ir asmenys, priskiriami sunkiausių ligos formų ar mirties rizikos grupėms. Lietuvoje tai buvo medikai, vyriausiojo amžiaus bei tam tikromis ligomis sergantys asmenys. Ši strategija yra labai svarbi programos pradžioje, tai yra strategija, nukreipta į asmens apsaugą, tačiau plečiantis skiepijimų galimybėms (didėjantis vakcinos tiekimas, skiepijimui būtinų infrastruktūrų sukūrimas) ir augant skiepijimo apimtims, tikslai ir uždaviniai keičiasi, pereinama prie visuomenės imuniteto formavimo etapo.
Nors šiuo etapu dėl įvairių priežasčių nepaskiepytiems prioritetinių grupių asmenims turi būti teikiama pirmenybė, skiepijimai neturi apsiriboti tik šiomis grupėmis. Tik esant pakankamai dideliam visuomenės imunitetui, galima tikėtis sukėlėjo, šio atveju – SARS-CoV-2 viruso, sumažėjusio cirkuliavimo visuomenėje. Tai leistų saugiai mažinti taikomų plitimo būdų kontrolės priemonių (karantino) apimtis. Plačiąja prasme kalbėtume apie tikslą pasiekti visos Lietuvos gyventojų 60–70 % visuomenės (kolektyvinį) imunitetą, tačiau tam būtina išnaudoti visas galimybes ir kaip galima greičiau sukurti kolektyvinį imunitetą ir mažesniuose kolektyvuose ar vietovėse. Kaip modelį būtų galima paminėti sporto klubą, kurį lanko santykinai nedidelis nuolatinių narių skaičius. Paskiepijus šio klubo personalą ir lankytojus, galima pasiekti beveik 100 % tokio kolektyvo imunitetą ir taip sudaryti savotišką „saugumo salelę“, atveriančią galimybę tokiam kolektyvui saugiai grįžti prie beveik įprasto veiklos režimo. Panašiai būtų galima kalbėti apie nedideles administracines teritorijas. Tokiam mažesnių kolektyvų skiepijimui būtų galima kooperuoti ne tik sveikatos sistemos, bet ir kitus resursus, būtinus
skiepijimo organizavimui, medikų papildomo darbo apmokėjimui ir kt. Tai įmanoma tik turint pakankamus vakcinų resursus. Perėjimas prie visuomenės imuniteto kūrimo strategijos leistų lanksčiau panaudoti turimus resursus, greičiau pasiekti „saugumo salelių“, o jų skaičiui augant – ir visos šalies saugumą. Žinoma, svarbu visuomenės imunitetą pasiekti kuo greičiau, tačiau kalbant apie terminus ir vertinant visas aplinkybes, būtų gerai užsibrėžtą tikslą pasiekti iki šių metų rudens, skaičiuojant paskiepytųjų pagal reikalavimus (2 dozės) 60–70 % apimtis, kai po vasaros atoslūgio vėl didės SARS-CoV-2 sezoninio aktyvumo augimo grėsmė.
Apie trečiąjį plačios apimties skiepijimo programos etapą – aukšto visuomenės imuniteto
palaikymą – šiandien galima kalbėti tik teoriškai. Reikia dėti visas pastangas, kad būtų sukurtas tinkamas visuomenės imuniteto lygis. Šiandien dar negalima vertinti vakcinų sužadinto apsauginio imuniteto trukmės ir sustiprinančių vakcinos dozių poreikio. Dar nežinoma, kokį poveikį šiems procesams turės atsirandančios naujos mutavusios SARS-CoV-2 padermės.
Visomis šiomis kryptimis vyksta intensyvūs moksliniai darbai ir jų rezultatai lems ateities
COVID-19 valdymo strategijas.
COVID-19 ir sveikatos apsaugos sistemos resursai
COVID-19 poveikis sveikatos apsaugos sistemai yra susijęs su smarkiai išaugusiu ambulatorinių kontaktų skaičiumi bei padidėjusiomis hospitalizacijos apimtimis, kadangi net 5–7 %
COVID-19 pacientų hospitalizuojami į gydymo įstaigas. Mažiausiai 70 % COVID-19 stacionaro
lovų būtina įrengti deguonį, užtikrinti griežtą pacientų srautų kontrolę, darbuotojų apsaugą
ir reikšmingai išplėsti intensyvios terapijos lovų skaičių. Pandemijos piko metu ne mažiau
kaip 40 % visų sveikatos sistemos resursų panaudojama Covid-19 pacientų sveikatos priežiūrai, tačiau medicinos darbuotojai taip pat suserga. Tyrimai rodo, kad vidutiniškai Lietuvoje
COVID-19 infekcija persirgo 26,5 % ligoninių darbuotojų, o kai kur šis rodiklis siekė iki 60 %.
Infekcinių ligų gydytojų, epidemiologų ir infekcijų kontrolės specialistų trūkumas šalyje taip
pat prisideda prie pandemijos valdymo problemų. Daugelis jau išvardytų veiksnių taip pat
lemia reikšmingą kitų sveikatos priežiūros paslaugų apimčių sumažėjimą. COVID-19 sukeltai kolateralinei pažaidai ypač reikšmingas savalaikės pagalbos užtikrinimas širdies ir kraujagyslių, onkologinėmis ir psichikos ligomis sergantiems asmenims, todėl hospitalinį šalies
sveikatos sektorių būtina saugoti nuo staigaus perkrovimo. Vienas iš būdų tai pasiekti yra išvengiamų hospitalizacijų mažinimas. Optimizuota pagalba visose paslaugų teikimo grandyse sergantiesiems lėtinėmis neinfekcinėmis ligomis turi užtikrinti stabilios pacientų būklės
palaikymą, medikamentinio gydymo ir ambulatorinės priežiūros tęstinumą be lėtinių ligų
paūmėjimų, neturi blogėti lėtinių ligų kontrolės rodikliai, negali didėti gyvybei grėsmingų
įvykių skaičius (insulto, miokardo infarktų, staigių mirčių). Taikomos priemonės turi užtikrinti
optimalią ligų kontrolę ir racionalų bei efektyvų asmens sveikatos priežiūros paslaugų naudojimą atsižvelgiant į besikeičiančius pandemijos veiksnius, todėl privalome išnaudoti visą
turimą technologijų potencialą. Telemedicinos naudojimas virtualioms medicininėms konsultacijoms galėtų būti perspektyvi alternatyva kontaktinėms konsultacijoms.
COVID-19 ligos pasireiškimo formos ir jų gydymas
COVID-19 liga gali pasireikšti besimptome, lengva, vidutine, sunkia ir kritiškai sunkia ligos
forma. Dažniausi COVID-19 ligos simptomai yra karščiavimas (> 38°C 31–43 %), kosulys (46–
82 %) ir dusulys (iki 31 %). Kiti COVID-19 ligai būdingi simptomai (sindromai): raumenų skausmas, bendras silpnumas, sloga, gerklės skausmas, kai kuriems pacientams pasitaiko viduriavimas, gali būti uoslės ar skonio praradimas, COVID-19 ligai progresuojant gali išsivystyti
pneumonija, širdies ritmo sutrikimai, ūminis inkstų pažeidimas, ūminis respiracinio distreso
sindromas (ŪRDS), sepsis, septinis šokas. Sunkios COVID-19 ligos formos rizikos veiksniai yra
vyresnis amžius (> 65 m.), lėtinės ligos (cukrinis diabetas, širdies ir kraujagyslių, kvėpavimo
takų ir kt.).
COVID-19 ligos klinikiniai sindromai ir juos apibūdinantys požymiai:
1 Lengva COVID-19 ligos forma pasižymi nespecifiniais simptomais – karščiavimu, kosuliu, gerklės skausmu, nosies užburkimu, silpnumu, galvos, raumenų skausmu, uoslės
ar skonio praradimu, gali pasireikšti gastrointestiniai simptomai: pykinimas, vėmimas,
viduriavimas. Vyresniems ir imunosupresuotiems pacientams simptomai gali būti atipiniai.
2 Nesunki ar vidutinio sunkumo pneumonija – kai nėra sunkios pneumonijos požymių
ir gydymo deguonimi poreikio (SpO2 ≥ 94 % kvėpuojant aplinkos oru). Vaikams pasireiškia karščiavimu, kosuliu ir (ar) pasunkėjusiu kvėpavimu bei tachipnėja (iki 2 mėn.
amžiaus – kvėpavimo dažnis ≥ 60 k/min., 2–11 mėn. – 50–59 k/min., 1–5 m. amžiaus –
40–49 k/min., vyresniems kaip 5 m. amžiaus > 30 k/min.), nėra sunkios pneumonijos
simptomų.
3 Sunki pneumonija suaugusiesiems ir paaugliams pasižymi karščiavimu arba įtariama
kvėpavimo takų infekcija ir yra bent vienas iš šių požymių: kvėpavimo dažnis > 30 k/
min., apsunkintas kvėpavimas arba nustatoma SpO2 < 94 % kvėpuojant oru, PaO2
/
FiO2 < 300 mmHg; infiltracija plaučiuose apima > 50 % plaučių audinio. Vaikams (nuo
gimimo iki 10 m. amžiaus) pasireiškia kosuliu ar pasunkėjusiu kvėpavimu ir yra bent
vienas iš šių simptomų: centrinė cianozė arba SpO2
< 90 %; sunkus kvėpavimo sutrikimas (pvz., intensyvus pagalbinių kvėpavimo raumenų darbas, tachipnėja) ir bendri
sunkios būklės požymiai: negalėjimas žįsti krūties ar gerti, mieguistumas ar sąmonės
sutrikimas, traukuliai.
4 ŪRDS diagnozuojamas tuomet, kai nauji simptomai ar būklės blogėjimas pasireiškia per
savaitę nuo ligos pradžios. Krūtinės ląstos radiologiniuose tyrimuose (rentgenogramoje, KT tyrimo vaizde, plaučių ultragarsinio tyrimo vaizde) nustatomi abipusiai pritemimai, kurių priežastis nėra hipervolemija, skilčių ar viso plaučio atelektazės, skystis pleuroje ar tumoras. Rekomenduojamas echokardiografijos tyrimas hidrostatinei edemos priežasčiai paneigti, jeigu jai nėra aiškaus rizikos veiksnio. ŪRDS klasifikacija
pagal oksigenaciją (ventiliuojant su PEEP ar CPAP ≥ 5 mmH2
O arba netaikant ventiliacijos):
a. lengvas: 200 mmHg < PaO2 / FiO2 ≤ 300 mmHg;
b. vidutinis: 100 mmHg < PaO2 / FiO2 ≤ 200 mmHg;
c. sunkus: PaO2 / FiO2 ≤ 100 mmHg;
d. kai nėra PaO2
duomenų, SpO2 / FiO2 ≤ 315, rodo, kad gali būti ŪRDS
(ir netaikant ventiliacijos).
5 Sepsis yra gyvybei pavojinga organų disfunkcija, kurią sukelia neadekvati organizmo
reakcija į įtariamą ar patvirtintą infekciją. Sunki infekcijos eiga nustatoma remiantis
qSOFA kriterijais (bent du iš trijų paminėtų): arterinė hipotenzija (sistolinis kraujospūdis ≤ 100 mmHg), sąmonės sutrikimas (pagal Glazgo komos skalę < 15 balų), tachipnėja
(kvėpavimo dažnis ≥ 22 k/min.). Organų disfunkcijos (kraujotakos, kvėpavimo, inkstų,
kepenų, kraujodaros, centrinės nervų sistemos) nustatomos remiantis SOFA (nuolatinio organų nepakankamumo vertinimo) skalės kriterijais. Organų disfunkcijos požymiai: pakitusi sąmonės būklė, pasunkėjęs kvėpavimas, tachipnėja, žema deguonies saturacija, sumažėjęs šlapimo išsiskyrimas, tachikardija, silpnas pulsas, šaltos galūnės ar
žemas kraujospūdis, marmurinė oda ar laboratorinių rodiklių pokyčiai: koagulopatija,
trombocitopenija, acidozė, hiperlaktatemija arba hiperbilirubinemija.
6 Sepsinis šokas suaugusiesiems yra išliekanti hipotenzija, nepaisant infuzoterapija koreguotos hipovolemijos, vazopresorių poreikis, siekiant išlaikyti vidurinį kraujospūdį
≥ 65 mmHg ir laktatų koncentraciją kraujyje > 2 mmol/l. Sepsinis šokas vaikams – hipotenzija (sistolinis kraujo spaudimas <5-os procentilės ar > 2 SD (standartinis nuokrypis)
žemiau amžiaus normos) arba 2 ar 3 iš šių simptomų: sąmonės sutrikimas, tachikardija
ar bradikardija (ŠSD < 90 k/min. ar >160 k/min. kūdikiams; ŠSD < 70 k/min. ar >150 k/
min. vaikams); pailgėjęs kapiliarų prisipildymo laikas (> 2 sek.) ar vazodiliatacijos epizodai; tachipnėja; marmurinė oda ar petechinis bėrimas; padidėjęs laktato kiekis kraujyje; oligurija; hipertermija ar hipotermija.
Pagrindiniai COVID-19 ligos etapai ir gydymo principai
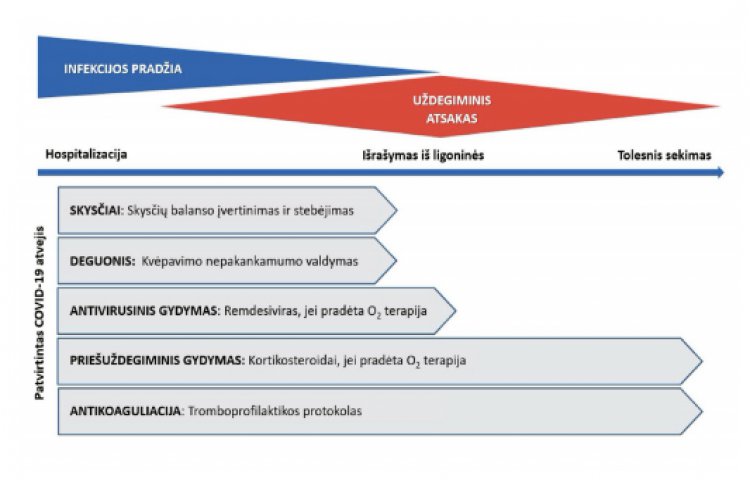

1 Remdesiviro dozavimas ir skyrimo ypatumai: Sol. Remdesiviri 200 mg su Sol. Na Cl 0,9 % – 250 ml per
120 min. į veną pirmą dieną, 100 mg su Sol. Na Cl 0,9 % – 250 ml per 60 min. į veną kitas 4 dienas.
Remdesiviro negalima skirti pacientams, kuriems gydymo pradžioje ALT aktyvumas ≥ 5 kartus viršija
viršutinę normos ribą.
Remdesiviro vartojimą reikia nutraukti, jeigu gydymo remdesiviru metu ALT aktyvumas ≥ 5 kartus
viršija viršutinę normos ribą (jį galima vėl paskirti, kai ALT aktyvumas < 5 kartus viršija viršutinę normos
ribą), padidėjus ALT aktyvumui atsiranda kepenų pažeidimo požymių ar simptomų arba didėja konjuguoto
bilirubino kiekis, šarminės fosfatazės aktyvumas arba tarptautinis normalizuotas santykis (TNS).
Prieš pradedant gydymą remdesiviru ir jį skiriant reikia vertinti aGFG. Remdesiviro negalima skirti
pacientams, kurių aGFG < 30 ml/min. Nėščiosioms remdesiviras turi būti skiriamas tik tais atvejais, kai
nauda viršija riziką.
2 Deksametazono dozavimas ir skyrimo ypatumai: Dexamethasone 6 mg/d per os arba Dexamethasone
sodium phosphate 8 mg į veną iki 10 d. arba iki išrašymo iš stacionaro, atsižvelgiant į aplinkybes. Nesant
galimybės skirti deksametazono, skirti prednizoloną, metilprednizoloną ar hidrokortizoną ekvivalentinėmis
dozėmis: 40 mg/d. prednizolono, 32 mg/d. metilprednizolono, 160 mg/d. hidrokortizono.
3 Sprendimą dėl remdesiviro skyrimo pacientui, kuriam taikoma DPV ir EKMO, priima gydytojas
anesteziologas reanimatologas, pasikonsultavęs su infekcinių ligų gydytoju ar gydytoju pulmonologu.
COVID-19 gydymo taktikos parinkimas pagal deguonies poreikį
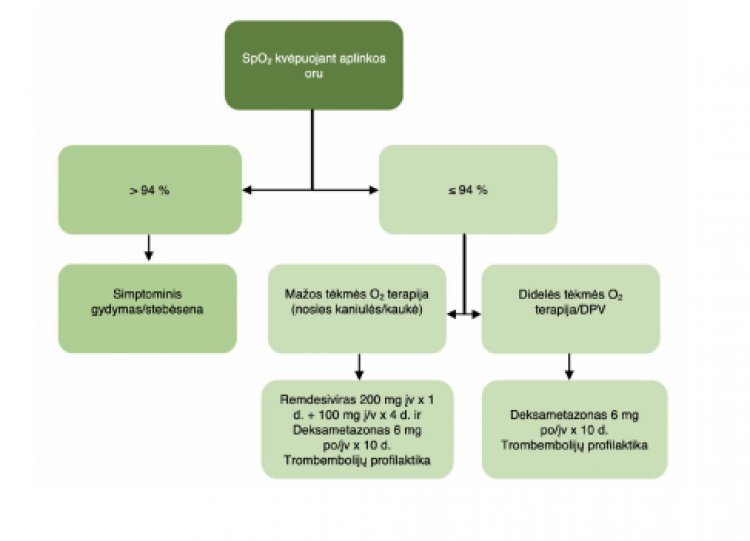
Kiti COVID-19 ligos gydymo metodai

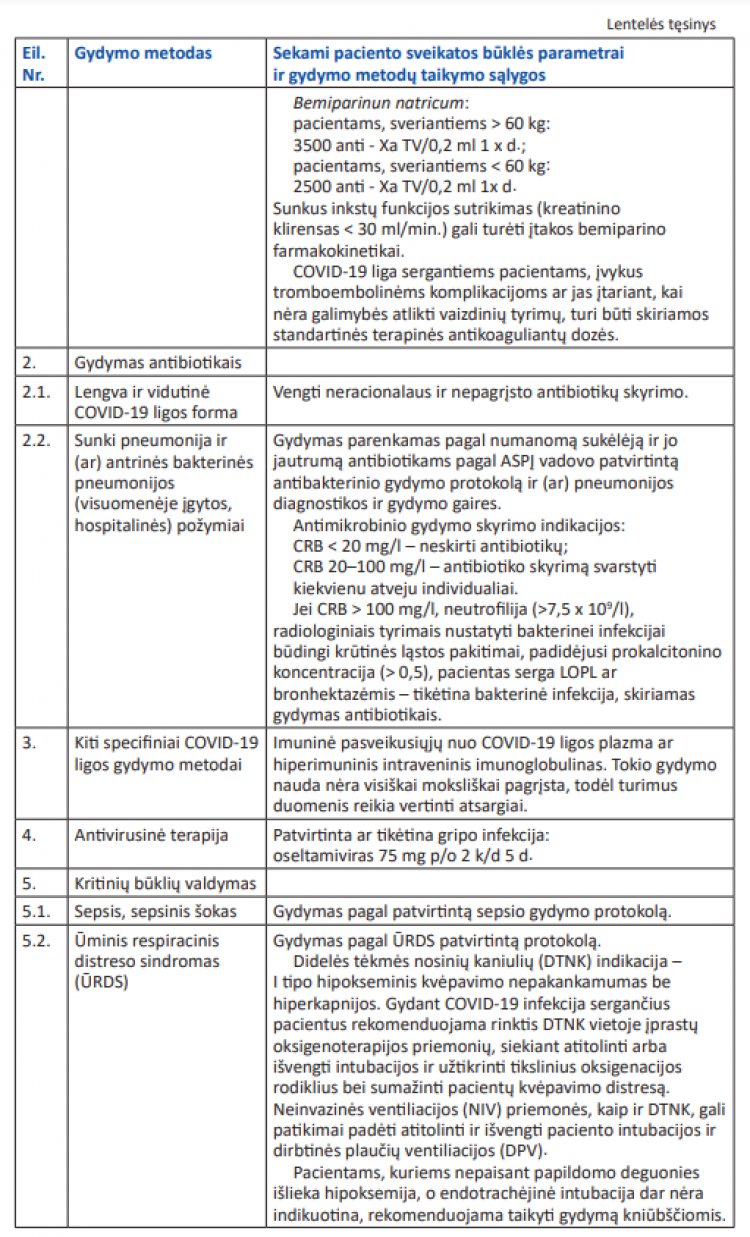

Nėščiosios, kuriai diagnozuota COVID-19 liga, gimdymo būdas parenkamas individualiai.
Sprendimą dėl suaugusių pacientų gydymo reanimacijos ir intensyviosios terapijos padalinyje priima gydytojas anesteziologas reanimatologas. Suaugusieji gydomi reanimacijos ir
intensyviosios terapijos padalinyje, kai:
1 skiriant kvėpavimo funkciją koreguojantį gydymą, nepavyksta pasiekti tikslinių oksigenacijos rodiklių;
2 pacientui reikalingas gydymas dirbtine plaučių ventiliacija;
3 išsivysto šokas;
4 išsivysto kritinė būklė sutrikus organų sistemų funkcijoms.
Vaikai gydomi vaikų intensyviosios terapijos skyriuje, kai:
1 deguonies terapijos poreikis > 9 l/min. (arba > 60 % FiO2
), kai SpO2
ar SaO2
< 90–92 %
(yra didelės tėkmės deguonies, CPAP ar kito neinvazinės ventiliacijos metodo poreikis
arba mechaninės ventiliacijos poreikis);
2 progresuojantys klinikiniai kvėpavimo nepakankamumo požymiai ir SpO2
< 92 %, skiriant > 10 l/min. deguonies;
3 šokas, sepsis, kitų organų nepakankamumas.
Literatūra
Kučinskas V. Genetikos ir genomikos pagrindai. Vilnius: VU leidykla, 2012.
Zhou B., Thi Nhu Thao T., Hoffmann D. et al. SARS-CoV-2 spike D614G change enhances
replication and transmission. Nature 2021. https://doi.org/10.1038/s41586-021-03361-1
European Centre for Disease Prevention and Control. SARS-CoV-2 – increased circulation
of variants of concern and vaccine rollout in the EU/EEA, 14th update (15 February
2021). [Žiūrėta 2021-04-19]. Prieiga per internetą: https://www.ecdc.europa.eu/
sites/default/files/documents/RRA-covid-19-14th-update-15-feb-2021.pdf
Centers for Disease Control and Prevention. SARS-CoV-2 variant classifications and
definitions (24 March 2021). [Žiūrėta 2021-04-19]. Prieiga per internetą: https://www.cdc.
gov/coronavirus/2019-ncov/cases-updates/variant-surveillance/variant-info.html#print
Agency for Clinical Innovation: COVID-19 Critical Intelligence Unit. Living evidence –
SARS-CoV-2 variants. [Žiūrėta 2021-04-19]. Prieiga per internetą: https://aci.
health.nsw.gov.au/covid-19/critical-intelligence-unit/sars-cov-2-variants
Global Virus Network. CAL.20C (20C/S:452R; /B.1.429) “California” variant. [Žiūrėta
2021-04-19]. Prieiga per internetą: https://gvn.org/covid-19/california-variant/
Wölfel R, Corman VM, Guggemos W, et al. Virological assessment of
hospitalised patients with COVID-2019. Nature 2020.
Health Infomation and Quality Authority, Ireland. Evidence summary
for COVID-19 viral load over course of infection. 2020.
Sethuraman N, Jeremiah SS, Ryo A. Interpreting Diagnostic Tests for SARS-CoV-2.
JAMA. 2020; 323(22):2249–2251. https://doi.org/10.1001/jama.2020.8259
Laboratory testing for coronavirus disease (COVID-19) in suspected
human cases. Interim guidance 19 March 2020. WHO.
From Publicly Reported Confirmed Cases: Estimation and Application. Ann Intern Med 2020.
Findings from investigation and analysis of re-positive cases. http://www.kdca.go.kr/
board/board.es?mid=&bid=0030&act=view&list_no=367267&nPage=11
https://www.cdc.gov/coronavirus/2019-ncov/lab/resources/antigen-tests-guidelines.html
Laboratory Diagnostics and Testing Guidance for COVID-19 https://
emedicine.medscape.com/article/2500138 (Update Apr 02, 2021)

 Valandos
Valandos